- · 《中国处方药》栏目设置[06/30]
- · 《中国处方药》收稿方向[06/30]
- · 《中国处方药》投稿方式[06/30]
- · 《中国处方药》征稿要求[06/30]
- · 《中国处方药》刊物宗旨[06/30]
首个国产曲妥珠单抗正式在国内上市 复宏汉霖
作者:网站采编关键词:
摘要:近年来,复宏汉霖一直保持着高歌猛进的姿态,不断加速产品的研发进度,逐渐构画起一幅庞大的生物制药版图。去年2月,汉利康获批,实现了国产生物类似药零的突破,也推动公司正
近年来,复宏汉霖一直保持着高歌猛进的姿态,不断加速产品的研发进度,逐渐构画起一幅庞大的生物制药版图。去年2月,汉利康获批,实现了国产生物类似药零的突破,也推动公司正式开启商业化转型之路。
智通财经APP了解到,8月14日,复宏汉霖-B(02696)自主研发的核心产品曲妥珠单抗汉曲优?(HLX02,欧盟商品名:Zercepac?)正式获得国家药监局(NMPA)批准上市,用于治疗HER2阳性的早期乳腺癌、转移性乳腺癌和转移性胃癌。此前,汉曲优?(欧盟商品名:Zercepac?)已于今年7月正式获欧盟委员会(EC)批准,成为首个登陆欧洲市场的“中国籍”单抗生物类似药。
这是复宏汉霖创立以来第二款获批上市的产品,也是首个获批上市的国产曲妥珠单抗生物类似药。
一直以来,复宏汉霖在抗HER2产品的开发与布局都在国内保持相对领先状态,随着汉曲优?在国内外获批上市,复宏汉霖研发能力和商业化的可持续性也进一步得以验证,无疑赋予了公司更高的内在价值。在此关键节点,投资者可从国内市场空间,以及公司国际开发和商业化优势等角度,深入了解复宏汉霖巨大的升值潜力和明朗的投资前景。
庞大的未满足需求和市场增长潜力
生物医药投资的重要逻辑,在于研判公司对创新研发的投入力度,以及研发成果转化后的目标市场体量与占有能力。在此背景下,生物医药细分赛道的容量大小,也在一定程度上决定了公司的成长空间,同时也决定了投资者对公司的想象高度。
智通财经APP了解到,乳腺癌分别位居我国女性恶性肿瘤发病率和死亡率的第1位和第5位,而HER2阳性乳腺癌占全部乳腺癌患者的20%以上,患者群体庞大。中国新增乳腺癌病例预计将由2018年的约32.07万例增至2030年的约37.32万例。而在胃癌方面,中国胃癌新增病例则将由2018年的44.23万例增至2030年的61.38万例。
曲妥珠单抗是国际医学界一致推荐的HER2阳性乳腺癌和胃癌的标准治疗用药。智通财经APP了解到,原研曲妥珠单抗 (赫赛汀)是罗氏旗下最畅销的肿瘤产品之一,2002年进入中国,不过其药价对国内普通患者并不“友好”。
在汉曲优?获批之前近二十年时间内,国内上市的曲妥珠单抗仅有赫赛汀,庞大的治疗市场为罗氏带来了丰厚的利润,2018年赫赛汀在中国境内的销售额达到27亿元。
2017年7月,赫赛汀被纳入国家医保目录乙类范围,价格定为7600元;价格降低之后,赫赛汀虽然让更多乳腺癌患者可负担,也意味着药品放量急剧增加,随之而来的便是药品短缺问题。
资料显示,赫赛汀纳入医保之后,一度出现全国性缺货现象,部分患者被迫断药。在此背景下,国内急需国产曲妥珠单抗出现,增加抗HER2治疗选择,并保障稳定供货来源。
这一层面上,汉曲优?的获批上市意义非凡,不仅增加了医生的用药选择,有望满足了国内HER2阳性乳腺癌和胃癌患者庞大且迫切的用药需求,还有助于增强市场的良性竞争,节省国家医保支出。
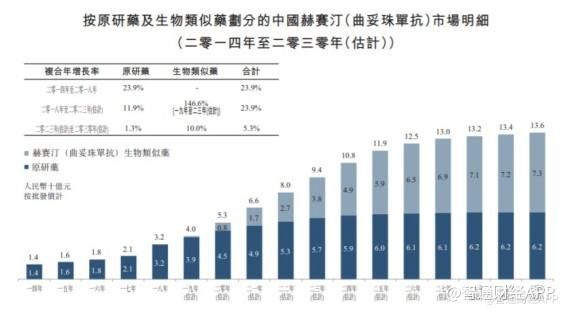
当然,汉曲优?获批上市,其意义不仅于此,还有望极大增厚复宏汉霖的利润空间。据智通财经APP了解,2020年,国内赫赛汀类似药市场规模仅有8亿元,但到2030年预计将达到73亿元。巨大的市场开发潜力,让复宏汉霖的价值曲线得到进一步攀升。
目前汉曲优?作为唯一上市的国产曲妥珠单抗,已处在国内赫赛汀类似药市场领先地位,且按照生物类似药平均审批时间来看,汉曲优?相比其他仍处于临床研究阶段的赫赛汀类似药至少具有1年半到2年的先发优势。
随着上市后国产替换进程不断加速,可以预见汉曲优?市场开发潜力巨大。这无疑将成为继汉利康之后,复宏汉霖开辟的又一片“变现”蓝海。
国际化开发为汉曲优?全球上市作好铺垫
近年来,复宏汉霖在不断丰富产品管线的同时,还积极推进国际化开发布局。正是得益于颇具前瞻性的高水平国际化战略布局,汉曲优?才能同时在国内外加速落地。
智通财经APP了解到,复宏汉霖建立了高效的一体化全球研发平台,公司分别在台北、上海及加州建立了三大研发中心,这三大研发中心密切合作,高效推动研发进展且兼顾成本效益。凭借多年的积累,复宏汉霖目前在海外的药政注册能力、临床开发和运营能力,可支持公司在全球多个地区开展临床试验。

其中,汉曲优?便是首个开展国际多中心III期临床研究的国产生物类似药。该临床试验结果在2019年于新加坡举办的ESMO Asia年会上发布。
文章来源:《中国处方药》 网址: http://www.zgcfyzz.cn/zonghexinwen/2020/0817/441.html
上一篇:医生处方药勿乱替换,看似只有一字之差,药效
下一篇:六张图表深度剖析非处方药市场